

蛍光とは
物質に紫外線を当てると発光する現象は、蛍石で初めて発見されました。そのため、蛍石の学名「フルオライト(fluorite)」にちなんで、このような現象を「フルオレッセンス(fluorescence)と呼びます。そして、フルオレッセンスの和訳が「蛍光」です。
漢字を見ると「蛍(ほたる)」の「光」ですが、昆虫のホタルの発光は、ルシフェリンという物質の化学反応による発光であり、紫外線とは関係がありません。現象に忠実に言うなら、蛍光は「蛍(ほたる)の光」ではなく「蛍石(ほたるいし)の光」です。
蛍光と言えば、身近なところでは「蛍光灯」が思い浮かびます。蛍光灯は、紫外線によって可視光を発生させる照明器具です。ガラス管の中はほぼ真空で、少量のアルゴンと水銀が入っており、放電が始まると中の水銀原子と電子が衝突します。そして、この衝突によって水銀原子から紫外線が放出され、ガラス管の内側に塗られた蛍光物質に紫外線が当たることにより、蛍光灯から可視光が発生します。
このように、蛍石で発見された蛍光、すなわち紫外線による発光現象は、身近なところでも利用されています。
蛍石が蛍光を放つしくみ
蛍石が紫外線によって発光するしくみは、基本的には電子の励起によって説明できます。ただし、蛍石(CaF2)の主成分であるカルシウムイオンやフッ化物イオンにおいて、電子が励起されるわけではありません。発光の中心となるのは、不純物として含まれる微量成分です。これを蛍光の「活性化因子(activator)」と呼びます。
蛍石の蛍光のうち、最も代表的なものは青紫色の光です。このタイプの蛍光は、多くの場合、希土類元素の1つであるユウロピウム(元素記号Eu、原子番号63)が活性化因子になっています。ユウロピウムは、2価の陽イオン(ユウロピウムイオン:Eu2+)の形で、蛍石を構成するカルシウムイオン(Ca2+)と部分的に置き換わっています。
蛍石が発する青紫色の蛍光は、波長420 nm(ナノメートル)付近にピークを持つ可視光です。この波長は、ユウロピウムイオンの基底状態の電子配置4f 7と、励起状態の電子配置4f 65d 1との間で電子が遷移するときの、エネルギーの大きさに対応しています。
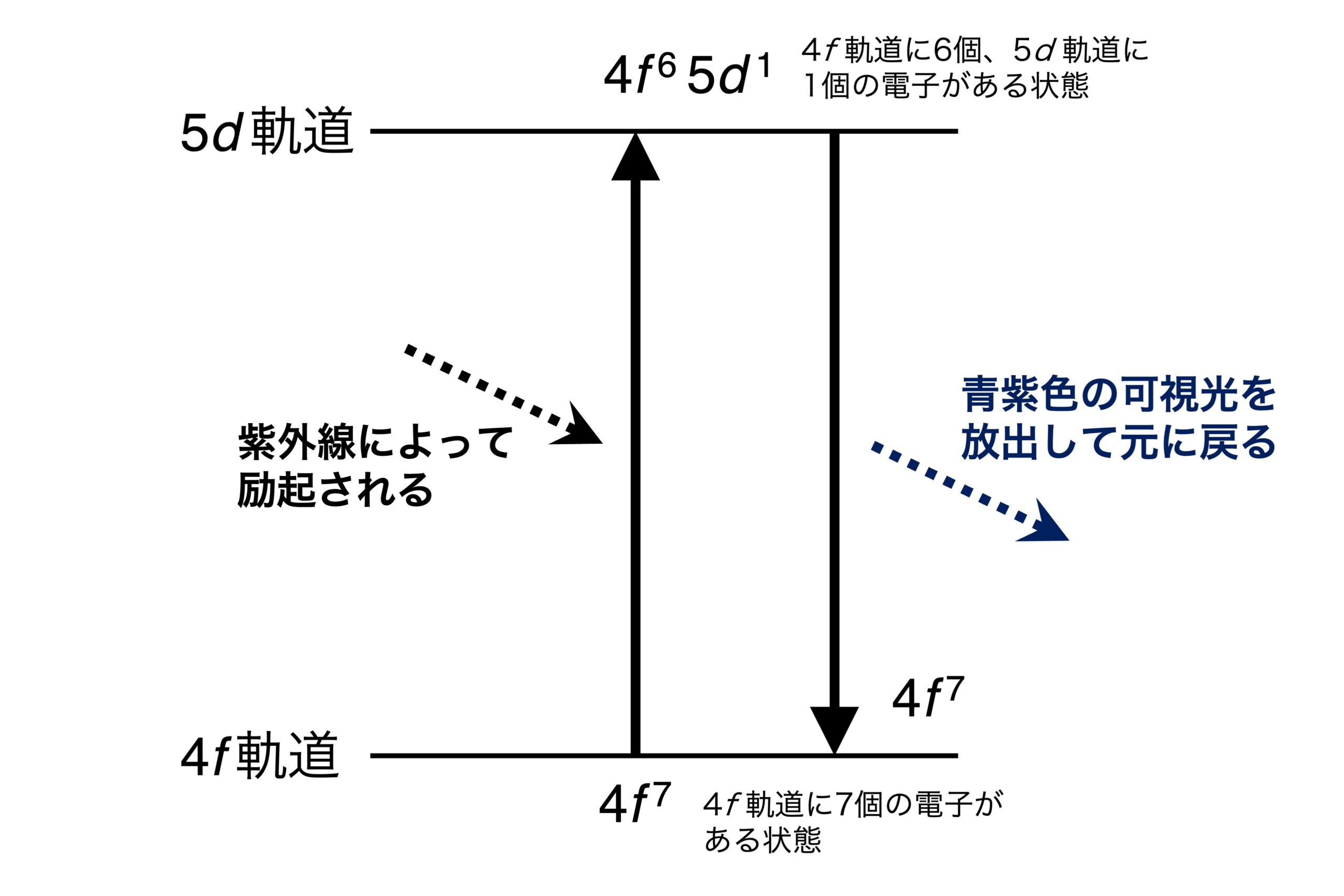
具体的に説明すると、蛍石に紫外線が当たることで、ユウロピウムイオンの4f 軌道にある電子が、一つ外側の5d 軌道へと励起されます。この電子は、紫外線のエネルギーを受けてより高いエネルギーの状態(励起状態)へと移行したことになります。その後、励起された電子はすぐに元の4f 軌道に戻ってしまうのですが、そのときに、持っていたエネルギーを光として放出します。これが蛍光の基本的なしくみです。
蛍光が観察できない時の原因と対策
蛍石の蛍光の観察は手軽にできる実験ですが、うまくいかないことも多々あります。その原因と対策を簡単にまとめます。
まず、紫外線ライトの波長が365 nm前後でないとよく見えません。安価な市販の紫外線ライトには、波長254 nm、波長365 nm、波長395 nmなどのタイプがあり、どの波長でも見えないことはないのですが、波長365 nmのタイプで典型的な青紫色の蛍光が見られる場合が多いです。
次に、蛍光は本当に暗い場所でないとよく見えません。暗幕などで部屋を真っ暗にして、さらに、黒い紙や布の上に蛍石を置いて紫外線ライトを当てるのがおすすめです。
最後に、すべての蛍石で蛍光が見られるわけではありません。ユウロピウムなどの微量成分(蛍光の活性化因子)を含む蛍石だけが蛍光を発するので、蛍光が見られない蛍石は意外に多くあります。
なお、ユウロピウム以外にも、ジスプロシウム、テルビウム、ネオジムなど多くの活性化因子が知られています。活性化因子が違うと、蛍光の色や強さも変わります。








