炭酸水素ナトリウムの水溶液が塩基性(アルカリ性)になるのは、炭酸水素イオン(HCO3-)が水と反応して炭酸を形成し、その過程で水酸化物イオン(OH-)が放出されるためです。
炭酸水素ナトリウムを水に溶かす場合、直感的にはナトリウムイオン(Na+)、水素イオン(H+)、炭酸イオン(CO3–)に分解されて酸性の水溶液になっても良さそうですが、実際にはそうなりません。
この記事では炭酸水素ナトリウムの水溶液が塩基性になる理由を、化学反応式を使って解説します。
▼▼▼参考動画▼▼▼
炭酸水素ナトリウムの化学式
炭酸水素ナトリウムとは、「炭酸」と「水素」と「ナトリウム」からなる物質です。
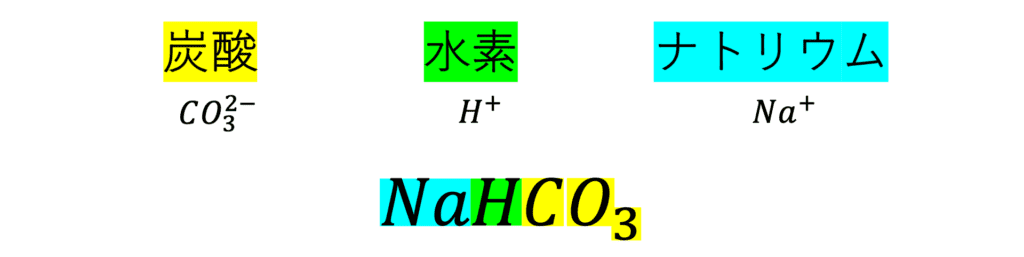
順番が後ろからですが、炭酸(CO3)、水素(H)、ナトリウム(Na)と、ちゃんと名前通りの化学式ですね。
ここからの説明は、この化学式を使って進めていきます。
炭酸水素ナトリウムを水に溶かした時のイオンの存在状態
まず、「炭酸水素ナトリウムを水に溶かす」を先ほどの化学式を使って表すと、次のようになります。
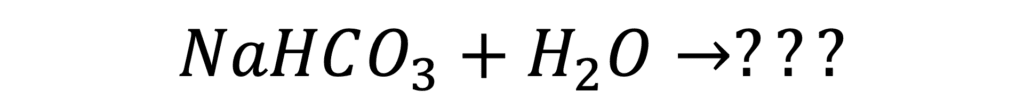
さあ、どうなるでしょうか。
炭酸水素ナトリウムは、水に溶けるといくつかのイオンに分解します。
重要なポイントは、その時に炭酸水素イオンができるということ。
次のような化学反応式で表すことができます。
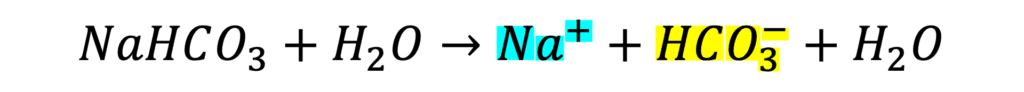
見てもらうとわかる通り、水素イオン(H+)や炭酸イオン(CO3–)はできずに、炭酸水素イオン(HCO3-)ができるのです。
これは炭酸水素ナトリウムの性質に由来するもので、炭酸水素ナトリウムは、水に溶けた時に水素イオンを放出しにくい炭酸水素塩なのです。
このことを「酸解離定数が大きい」と言います。
炭酸水素イオンは水分子と反応してOH-を放出する
先ほど示した通り、炭酸水素ナトリウムは水に溶けるとナトリウムイオンと炭酸水素イオンに解離します(①式)。
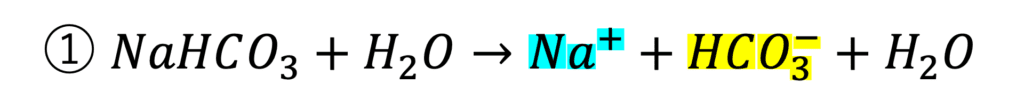
さて、その次です。
水溶液中の炭酸水素イオンは安定な状態ではないので、水と反応して炭酸(H2CO3)を形成します(②式)。
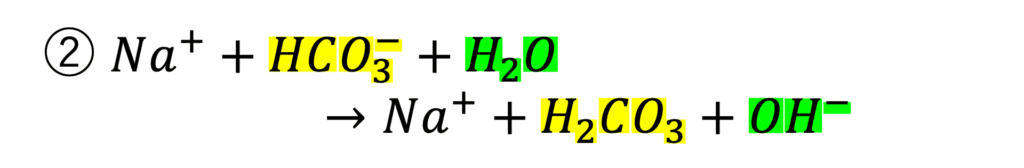
この過程で水酸化物イオン(OH-)が放出されるため、水溶液が塩基性になるのです。
ご存知の通り、水溶液中にOH-が増えれば塩基性(アルカリ性)、H+が増えれば酸性、ですね。
これが炭酸水素ナトリウムの水溶液が塩基性になる理由です。
なお、生じた炭酸(H2CO3)も安定ではないため、もう少し反応は進みます。
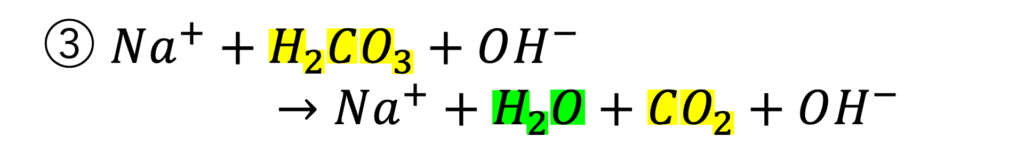
③式のように炭酸は水と二酸化炭素に分解され、最終的にこのようなイオンの存在状態になります。
まとめ
今回の内容で覚えておきたい重要なポイントは、以下の2点です。
- 炭酸水素ナトリウムは、水に溶けた時に水素イオンを放出しにくい炭酸水素塩である。(このことを「酸解離定数が大きい」と言う。)
- 炭酸水素イオンと水分子が反応して炭酸を形成し、その過程で水酸化物イオンが放出されるため、水溶液は塩基性(アルカリ性)になる。
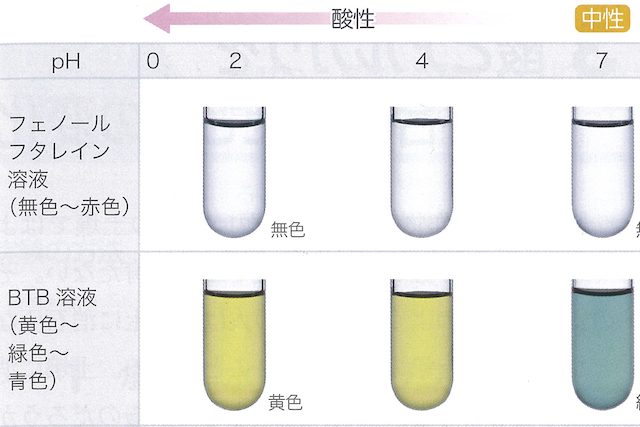
なお、炭酸水素ナトリウムの水溶液は、pH = 8.3程度の弱いアルカリ性です。
そのためpH指示薬として、弱アルカリを検出できるBTB溶液が用いられます。
読者からの質問
炭酸水素ナトリウム水溶液を放置しておくと、分解後は何になるのでしょうか?
【質問1】炭酸水素ナトリウム水溶液を常温で放置しておくと、分解後は「炭酸ナトリウム水溶液」になるのでしょうか。分解後に炭酸ナトリウム水溶液になっていないのなら、どんな物質になっているのでしょうか。
放置しておいても、「炭酸水素ナトリウム水溶液」
記事本文に示した化学反応式①〜③は、
固体成分が全部溶けたとして、水溶液中のイオンを考えると、
Na+、HCO3-、CO3–、OH-
となります。
つまり、③式の反応でCO2が発生するものの、水溶液の中には依然として「炭酸水素イオン(HCO3-)」
ですので、反応後も「炭酸水素ナトリウム水溶液」
また、炭酸水素イオンの一部は「炭酸イオン(CO3–)」
多くは炭酸水素イオンとして存在しますが、「中には炭酸イオンとして存在しているものもある」という感じです。
この辺のイオンの存在状態については、
入浴剤として重曹を入れたお風呂は、「炭酸ナトリウム風呂」になるのでしょうか?
【質問2】入浴剤としてお風呂に重曹を入れる場合がありますが、
お風呂からは二酸化炭素が発生し、お湯は弱酸性で、その中には炭酸水素イオンやナトリウムイオンなどが溶けています
つまり、「炭酸水素ナトリウム風呂」です。
詳しくは【
炭酸水素ナトリウム水溶液が徐々に分解して、すべてが「炭酸ナトリウム水溶液」に変わるには、何日くらいかかるでしょうか?
【質問3】炭酸水素ナトリウム水溶液を放置しておくと徐々に分解していくと思うのですが、たとえば4%程度の炭酸水素ナトリウム水溶液を100mL作ったとき、すべてが「炭酸ナトリウム水溶液」または「水酸化ナトリウム水溶液」に変
「炭酸水素ナトリウム水溶液を放置しておくと徐々に分解していく」は、
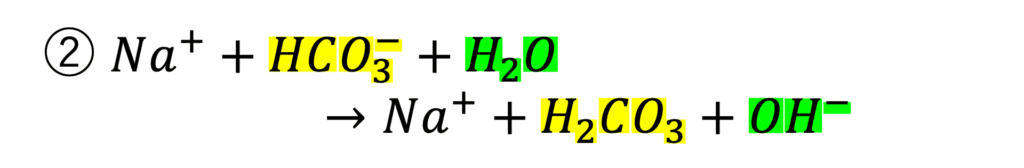
炭酸水素イオンと水が、加水分解によって、
ここでちょっと【質問1】の補足ですが、
これらは、水に溶けているという意味で「aq(アクア)」
つまり、加水分解の結果として③
HCO3-、CO3–、H2CO3(aq)、
という4種類の状態で存在しています。
そして、二酸化炭素がどれだけ出ていくかというのは、大気中の二酸化炭素濃度との平衡で決まります。
先ほどの4種類の存在形態でいえば、CO2(aq)と大気中の二酸化炭素(← CO2(g)と書きます。gは「ガス」の意味)との平衡が成り立っているという意味です。
当然ながら大気中の二酸化炭素は0%ではありませんので、どれだけ放置しておいても、水溶液から二酸化炭素(CO2(
したがって、炭酸水素イオンも無くなりません。
これらの理由から、「すべてが〇〇に変わるのは何日」